Ifølge en gruppe forskere fra University of Pennsylvania kan solens, vindens og havets kraft snart samles om at producere miljøvenligt brintbrændstof. Holdet integrerede vandrensningsteknologi i et nyt eksperimentelt projekt havvandselektrolysator, som bruger en elektrisk strøm til at adskille brint og ilt i vandmolekyler.
Ifølge Bruce Logan, professor i miljøteknik ved Kappa og professor ved Evan Pugh University, kunne denne nye metode til "havvandsspaltning" lette omdannelsen af vind- og solenergi til oplagbare og bærbare brændstoffer.
"Brint er et fantastisk brændstof, men du er nødt til at få det," sagde Logan. - Den eneste bæredygtige måde at gøre dette på er at bruge vedvarende energi og producere den fra vand. Du skal også bruge vand, som folk ikke vil bruge til andre formål, og det ville være havvand. Så brintproduktionens hellige gral skulle kombinere havvand, vind- og solenergi, der findes i kyst- og havmiljøer."
På trods af overfloden af havvand bruges det normalt ikke til vandseparation. Hvis vandet ikke afsaltes, inden det føres ind i elektrolysatoren – et dyrt ekstra skridt – bliver klorionerne i havvandet til giftig klorgas, som ødelægger udstyret og siver ud i miljøet.
For at forhindre dette indsatte forskerne en tynd, semipermeabel membran, der oprindeligt var designet til at rense vand i omvendt osmose (RO) behandling. Den omvendte osmose-membran har erstattet den ionbyttermembran, der almindeligvis anvendes i elektrolysatorer.
"Idéen bag omvendt osmose er, at du lægger virkelig højt tryk på vandet, skubber det gennem membranen og holder klorionerne bag," sagde Logan.
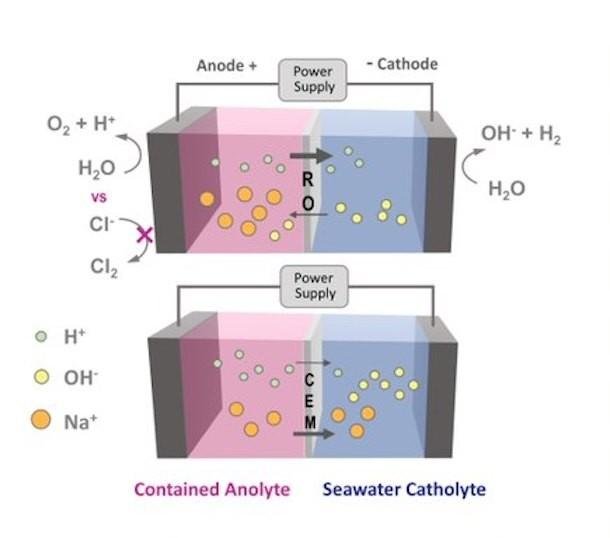
I elektrolysatoren vil havvand ikke længere trænge gennem den omvendte osmose-membran, men tilbageholdes af den. Membranen bruges til at adskille reaktioner, der forekommer nær to neddykkede elektroder - en positivt ladet anode og en negativt ladet katode - forbundet til en ekstern strømkilde. Når strømmen er tændt, begynder vandmolekyler at splitte ved anoden, frigive små brintioner kaldet protoner og danne iltgas. Protonerne passerer derefter gennem membranen og kombineres med elektroner ved katoden for at danne brintgas.
Med en omvendt osmosemembran installeret forbliver havvandet på katodesiden, og klorionerne er for store til at passere gennem membranen og nå anoden, hvilket forhindrer dannelsen af klorgas.
Men ved vandspaltning, som Logan påpegede, opløses andre salte bevidst i vandet for at gøre det ledende. Ionbyttermembranen, som filtrerer ioner ved elektrisk ladning, tillader saltioner at passere gennem den. Der er ingen omvendt osmose membran.
Fordi bevægelsen af større ioner er begrænset af RO-membranen, var forskerne nødt til at teste, om de små protoner, der bevægede sig gennem porerne, var nok til at opretholde en høj elektrisk strøm.
I en række eksperimenter testede forskerne to kommercielt tilgængelige omvendt osmosemembraner og to kationbyttermembraner, en type ionbyttermembran, der tillader bevægelse af alle positivt ladede ioner i systemet. Hver af dem blev testet for membranens modstand mod bevægelser af ioner. Mængden af energi, der var nødvendig for at fuldføre reaktionerne, blev også beregnet, dannelsen af gasformig brint og oxygen blev overvåget, interaktionen med chlorioner og beskadigelse af membranen blev analyseret.
Forskerne modtog for nylig en bevilling på $300 fra National Science Foundation (NSF) til at fortsætte forskningen i havvandselektrolyse. Logan håber, at deres forskning vil spille en afgørende rolle i at reducere udledningen af kuldioxid på verdensplan.
Læs også:
